第274回関東甲信越地方会 受賞者一覧(2024年12月14日開催)
第274回関東甲信越地方会 最優秀賞受賞演題(2024年12月14日開催)
Student Award
冠攣縮の関与が推察される突然死例の心外膜冠動脈と心筋間小動脈の病理形態異常
山近 萌恵乃1)2), 松山 高明2),中村 恵里2)3),曽根 浩元2)3), 森 敬善3), 小川 高史4), 鈴木 洋3)
1) 昭和大学 医学部 医学科
2) 昭和大学 医学部 法医学講座
3) 昭和大学藤が丘病院 循環器内科
4) 昭和大学藤が丘病院 臨床病理診断
【背景】
攣縮を生じた心外膜冠動脈では、粥状硬化病変の有無に関わらず、攣縮の繰り返しによる中膜の肥厚1)や新生内膜の増生2)3)をみることがある。しかし、末梢の心筋間小動脈を含めた冠動脈の形態異常との関連は明らかではない。今回、突然死に冠攣縮が関与したと推察される2解剖例について、心筋間小動脈を含めた冠動脈の病理形態を検討した。
【症例】
〈症例1〉40代女性。新型コロナウイルスワクチン接種後の副反応(発熱)で一時降圧薬を休薬していた。早朝に胸痛が出現し、心室細動(VF)から心肺停止(CPA)となり翌日死亡した。〈症例2〉50代女性。午前中駅で意識消失し、VF, CPAとなり3日後に死亡した。
【結果と考察】
2 例ともに梗塞部は各冠動脈の支配領域に相当していたが、各症例の心外膜冠動脈の狭窄の程度には一致していなかった。冠攣縮による病理形態異常として、心外膜冠動脈では全周性、線維性の内膜肥厚や、肥厚した内膜が不規則に縮み鋸歯状を呈する像がみられ(図1)、より末梢の動脈(図2)および心筋間の小動脈(図3)では内膜とともに中膜にも壁肥厚がみられた。冠攣縮によりこのような変化が起こる機序として、冠攣縮が起こった際の血流減少や内膜損傷による局所血栓の形成が関与していると考えられ4)、血栓が器質化されることで線維層が形成され、これを繰り返すことで内膜が多層性肥厚を示す可能性が考えられた
【結語】
心筋壊死を伴う突然死例では、心外膜冠動脈の内膜肥厚や心筋間の小動脈の壁肥厚が目立つ場合は、冠攣縮の可能性も考慮すべきと考えられる。
【参考文献】
- 1)
- Nakamura T, et al. Structural Thickening of Medial Layer in Coronary Artery With Spasm in Patients With Myocardial Infarction: J Am Heart Assoc 2021; 10: e018028.
- 2)
- Suzuki H, et al. Histological Evaluation of Coronary Plaque in Patients With Variant Angina: Relationship Between Vasospasm and Neointimal Hyperplasia in Primary Coronary Lesions: J Am Coll Cardiol 1999; 22: 198-205.
- 3)
- 阿部芳久ら. 冠攣縮狭心症の病理組織学的検討: 心臓 1995; 27(suppl): 8-12.
- 4)
- Nishi T, et al. Layered Plaque in Organic Lesions in Patients With Coronary Artery Spasm: J Am Heart Assoc. 2022; 11: e024880.
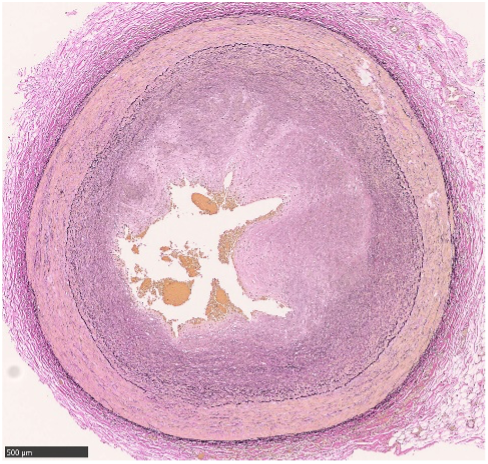
図 1. 症例2: 心外膜右冠動脈(#4) (Elastica van Gieson染色)
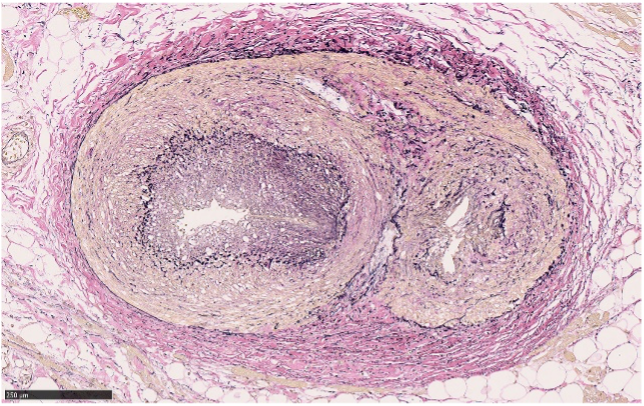
図 2. 症例1: 心外膜末梢 (房室結節動脈) (Elastica van Gieson染色)
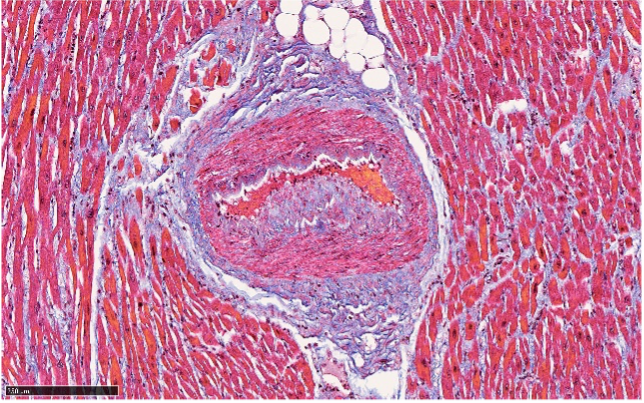
図3. 症例 2: 左室前壁中隔心筋間小動脈 (Masson’s trichrome染色)
Resident Award
経皮的左心耳閉鎖術後の医原性重度ARに対して外科手術を施行した一例
神谷寛登, 中永寛, 西村承子, 植木力, 佐藤敦彦, 松山重文, 田端実
虎の門病院 循環器センター外科
【症例】
症例は57歳男性. PAFに対するカテーテルアブレーション後の方で, 経皮的左心耳閉鎖デバイスの治験に参加し, 他院で経皮的左心耳閉鎖術が施行された. 術後, デバイスが左室内に脱落したため, 大動脈弁越しにデバイスの回収操作が行われた. しかし, 回収操作に伴い医原性重度ARが生じ, 労作時息切れが出現. 低侵襲手術の検討目的で当科紹介となった.
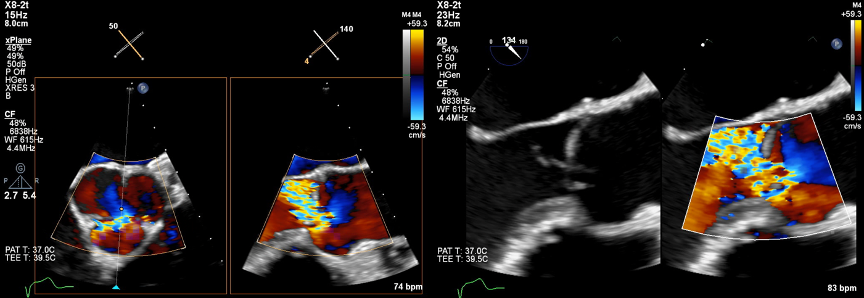
術前の経胸壁心エコーでは, LVDd/LVDsは56/34mm, LADは40mm, EFは66%, 右冠尖逸脱による重度AR を認めた. 経食道心エコーでは右冠尖の交連部断裂を伴う重度AR (Figure. 1), 約3.8mm大のBrockenbrough法による医原性ASD, 及び偶発的にPFOを認めた.
症候性重度AR及びASD, PFOに対して, 胸腔鏡下大動脈弁置換術, ASD閉鎖術, PFO閉鎖術を行った.
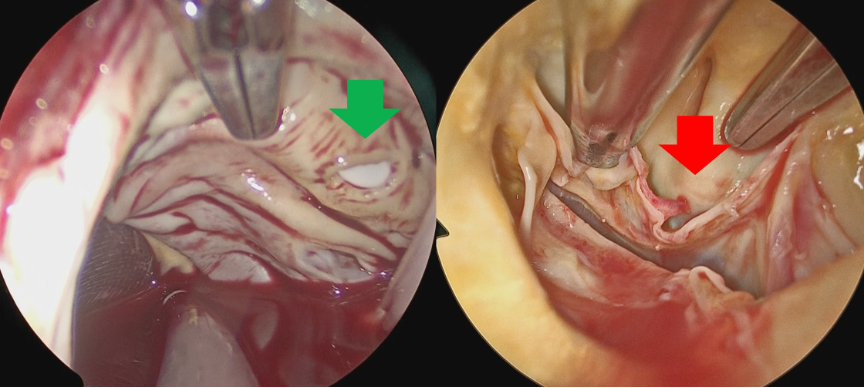
術中所見 (Figure. 2) では, 2カ所の医原性ASDとPFOを認め, それぞれ縫合閉鎖した. 大動脈弁は3尖で, RCC基部がRN交連部より1/2ほど裂けており, 同部が左室側に翻転していた. 本人の希望に沿って生体弁で置換した. 術後経過は良好で, 術後5日目に退院となった.
【考察】
経皮的左心耳閉鎖デバイスの脱落頻度は0.6%-3.9%と報告されている.1, 2
また, ドイツからの多施設データを分析した論文3によると, デバイス脱落例は108例報告されており, 本症例のように左室に脱落した症例の割合は33.3%と, 脱落箇所として2番目に多いとされている. これらの脱落に対する対処法としては, カテーテルによる回収が全体の75.0%と最も多く行われており, 左室への脱落例に対しては61.1%の症例でカテーテルによる回収が施行されている. 同論文内では, カテーテルでの回収症例全体においては経動脈的逆行性回収が54.3% と最多を占めていたが, 左室への脱落症例に対してどのような回収が行われたかは明らかでない. 本症例のように, 左室内に脱落したデバイスを回収する際には, 経動脈的逆行性の回収操作に伴って大動脈弁損傷が生じる可能性があり, 手術リスクが許容できる場合は外科的回収を行うのがよいと考えられる.
【結論】
経皮的左心耳閉鎖術時に脱落したデバイス回収の際に生じた医原性重度ARに対して, 胸腔鏡下大動脈弁置換術 + 医原性ASD + PFO閉鎖術を施行した. 左室に脱落したデバイスを経カテーテル大動脈アプローチで回収する際には, 大動脈弁損傷のリスクに留意する必要がある.
【参考文献】
- Saibal K, Shephal K, Ashish S, et al. Primary outcome evaluation of a next-generation left atrial appendage closure device: Results from the PINNACLE FLX trial. J Am Coll Cardiol. 2021;143(18):1754–1762. https://doi.org/10.1161/CIRCULATIONAHA.120.050117.
- Bajaj N, Parashar A, Agarwal S, et al. Percutaneous left atrial appendage occlusion for stroke prophylaxis in nonvalvular atrial fibrillation: A systematic review and analysis of observational studies. J Am Coll Cardiol Intv. 2014;7(3):296–304. https://doi.org/10.1016/j.jcin.2013.11.010.
- Eppinger S, Piayda K, Galea R. Embolization of percutaneous left atrial appendage closure devices: Timing, management and clinical outcomes. Cardiovasc Revasc Med. 2024;64:7–14. https://doi.org/10.1016/j.carrev.2024.02.014.
Clinical Research Award
心原性ショックを合併する急性冠症候群の予後:KiCS-PCIレジストリを用いた時系列トレンド解析
大畑 孝憲1, 香坂 俊1,中丸 遼2,白石 泰之1, 植田 育子1, 工野 俊樹3, 小平 真1, 小平 真幸1, 小野 智彦4, 沼澤 洋平1, 野間 重孝5, 家田 真樹1
1: 慶應義塾大学医学部循環器内科
2: 杏林大学医学部付属病院循環器内科
3: Division of Cardiology, Montefiore Medical Center, Albert Einstein College of Medicine
4: 国立病院機構埼玉病院循環器内科
5: 済生会宇都宮病院循環器内科
【背景】
心原性ショックを合併する急性冠症候群(CS-ACS)に対して生命予後改善のため緊急冠動脈インターベンション(PCI)が広く実施されているが、本邦での機械的補助循環(MCS)の使用率、院内死亡率を含む治療成績が経時的に改善しているかは不明である。
【方法】
Keio Interhospital Cardiovascular Studies (KiCS)-PCIレジストリを用いて、2009年から2019年の間にPCIを実施された24,527名の内、CS-ACS患者870名を対象に院内死亡率、機械的補循環の利用率、多枝病変を呈する患者に対する責任病変のみのPCI実施率、及びPCI後の合併症率に関して時系列トレンド解析を行った。
【結果】
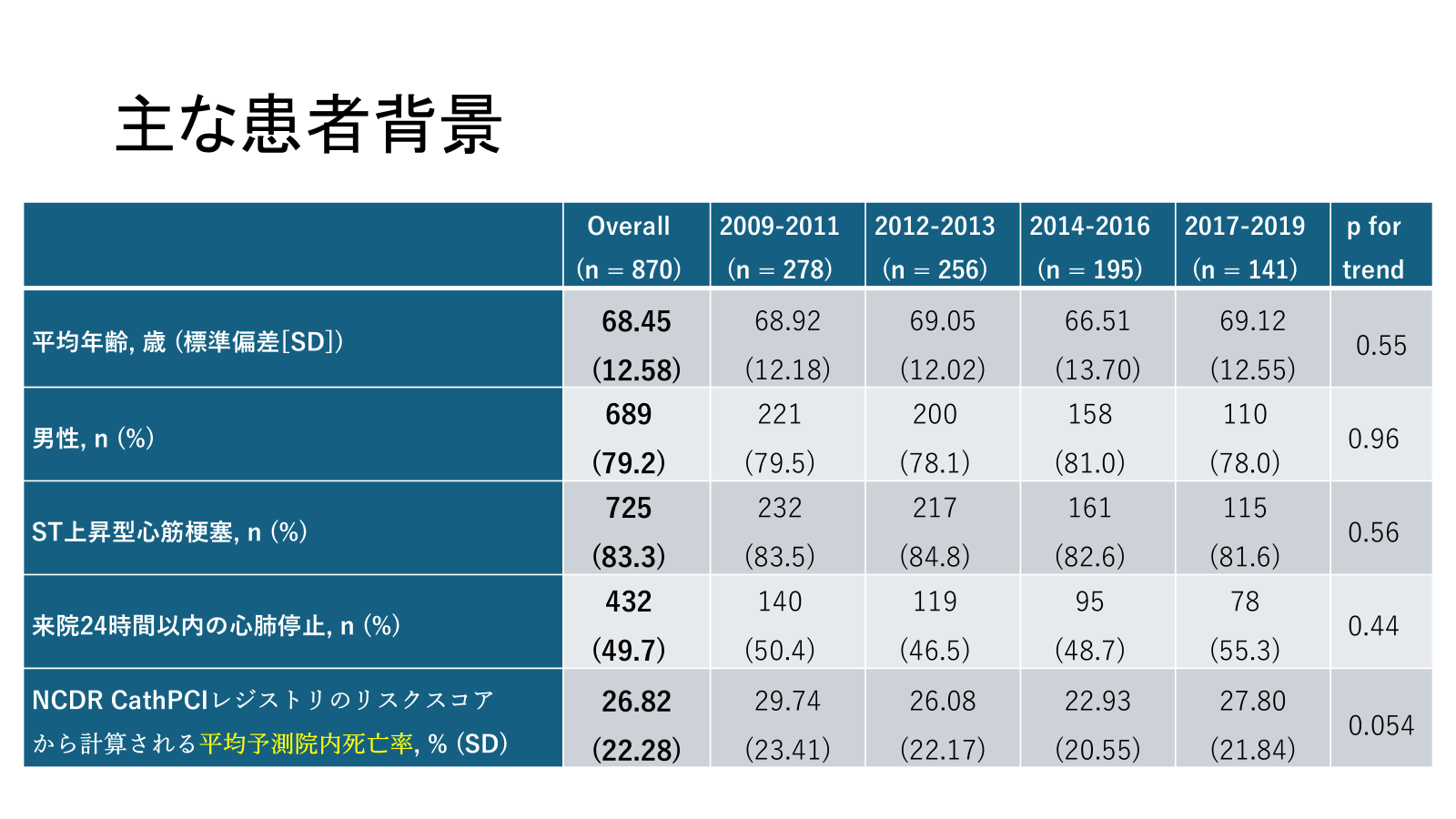
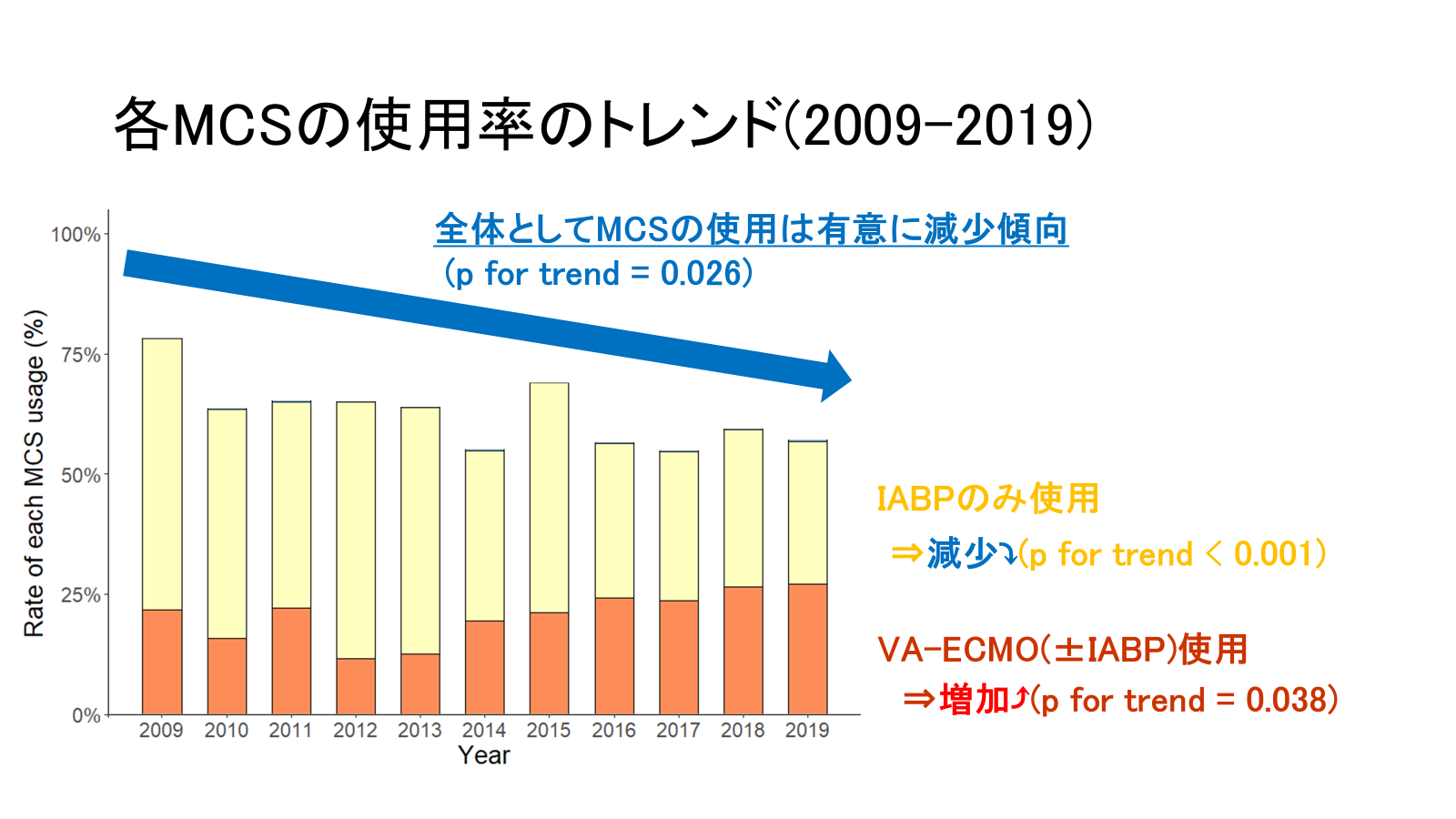
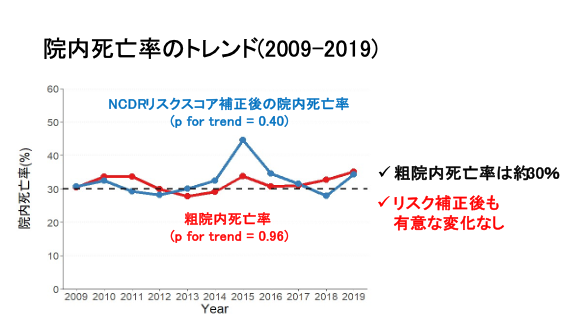
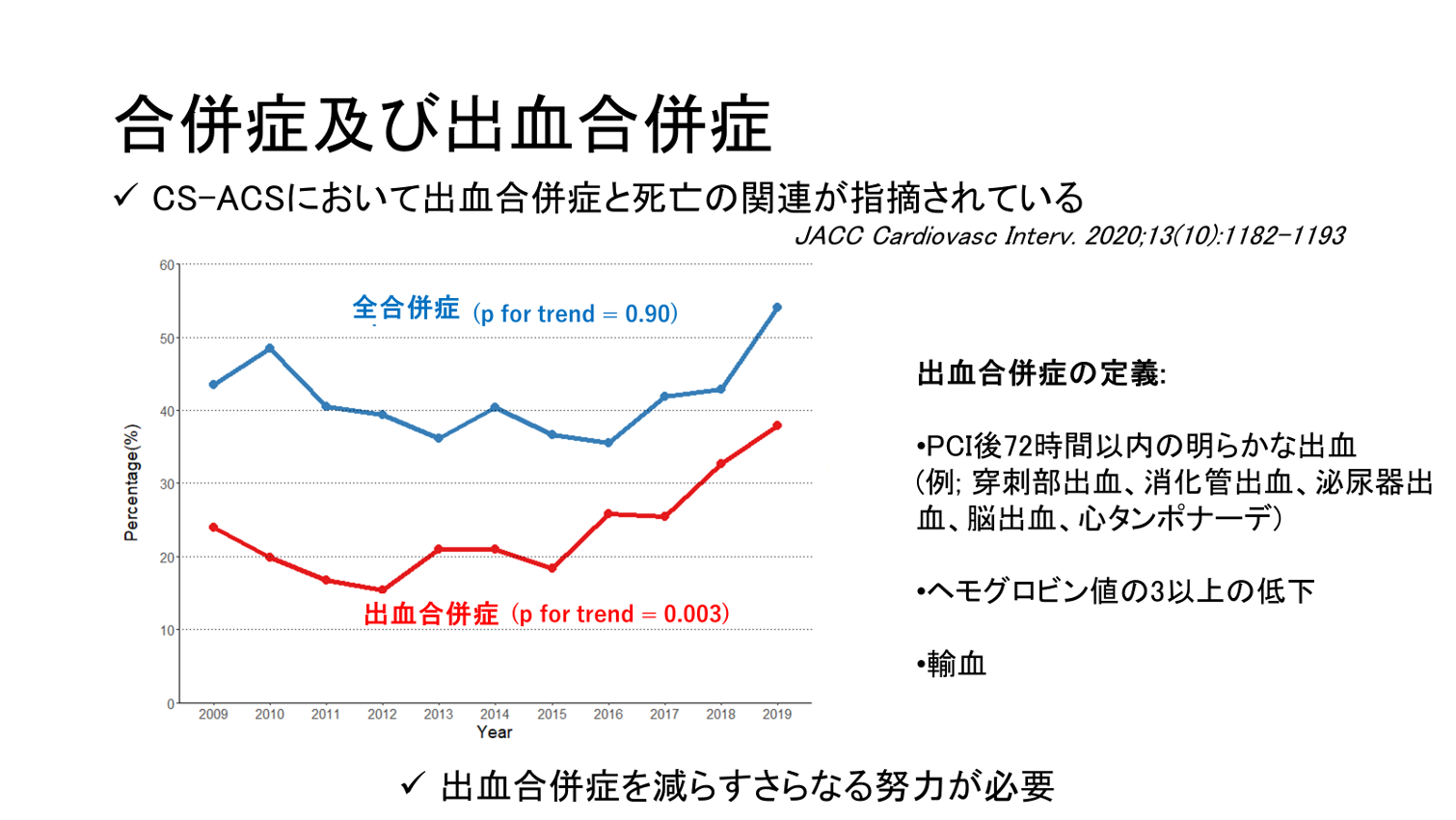
患者は平均年齢68.5歳、ST上昇型心筋梗塞が約8割、来院24時間以内の心肺停止が約5割を占めた(表1)。また、National Cardiovascular Data Registry (NCDR) CathPCIレジストリのリスクスコアから算出された予測院内死亡率は27%程度であり観察期間を通じて有意なトレンドは示さなかった(表1)。MCSに関して、体外式膜型人工肺(VA-ECMO)の使用率が有意に増加したが大動脈バルーンパンピング(IABP)の単独使用が大きく減少し、全体としてMCSの使用は減少した(図1)。粗院内死亡率は30%で横ばいであり、NCDRリスクスコアで補正後も同様の結果であった(図2)。多枝病変患者に対する責任病変のみのPCI実施率は70%程度で横ばいであり、PCI後の出血合併症が有意に増加傾向(図3)であった。
【考察】
IABPの利用率の顕著な減少は各国ガイドライン1-2)においてIABPのルーチン使用がClassⅢ推奨となったためと考えらえる。多枝病変患者に対する責任病変のみのPCIの実施もClassⅠ推奨1)であるが、観察期間中は横ばいであった。出血合併症は院内死亡との関連が報告されており3)、出血合併症が増えていることは重く受け止める必要がある。
【結論】
CS-ACSに対してPCIを実施された患者の院内死亡率は約30%程度で横ばいであった。患者予後改善のため、多枝病変患者に対する責任病変のみのPCIの実施率向上、出血合併症を防ぐさらなる努力が重要と考えられた。
【図表】
【参考文献】
- Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC Guidelines for the management of acute coronary syndromes [published correction appears in Eur Heart J. 2024 Apr 1;45(13):1145. doi: 10.1093/eurheartj/ehad870]. Eur Heart J. 2023;44(38):3720-3826. doi:10.1093/eurheartj/ehad191
- Kimura K, Kimura T, Ishihara M, et al. JCS 2018 Guideline on Diagnosis and Treatment of Acute Coronary Syndrome. Circ J. 2019;83(5):1085-1196. doi:10.1253/circj.CJ-19-0133
- Freund A, Jobs A, Lurz P, et al. Frequency and Impact of Bleeding on Outcome in Patients With Cardiogenic Shock. JACC Cardiovasc Interv. 2020;13(10):1182-1193. doi:10.1016/j.jcin.2020.02.042
Case Report Award
セレン欠乏により急激な心機能障害を呈し、その補充により改善が得られた一例
森泉友斉, 西山崇比古, 小室薫子, 平出貴裕, 岸野喜一, 白石泰之, 桃井瑞生, 遠藤仁, 林田健太郎, 鶴田ひかる, 香坂俊, 家田真樹
慶應義塾大学医学部 循環器内科
【症例】
クローン病の治療歴がある63歳男性。腎機能低下が顕著となり透析導入目的で入院した際、約3ヶ月間で左室駆出率(LVEF)が52から29%へ低下していた。身体所見に明らかな異常は無く、十二誘導心電図で広範な誘導に陰性T波を認めたが、冠動脈は正常であった。疾患特異的な異常所見は指摘されず、左心機能障害の診断に苦慮した。心筋症の診断ガイドラインに基づき鑑別を進める中で、セレン欠乏が鑑別疾患として挙げられた。改めて身体所見を確認すると爪白色化が認められ、また、小腸部分切除の既往があったことから、セレン欠乏症が疑われた。血清セレン値を測定すると5.8µg/dL(基準値: <10.0µg/dL)と低値であり、静脈投与によるセレン補充を開始した。1週間後には心機能は劇的に改善し、補充開始から10日後に自宅退院とした。退院3か月後にはLVEFは50%に回復した。また、爪の白色化や心電図変化も改善を認めた。
【考察】
セレンは必須微量元素の一つであり、その欠乏は拡張型心筋症を引き起こし、重篤化すると致死的となる可能性もある。一般に長期間の経腸・経静脈栄養を受けている患者に多く見られるが、クローン病や腸管切除後でもセレン欠乏が報告されている。また、腎不全や透析患者においては、低栄養、食事制限、消費亢進などが原因で血中セレン濃度が低下すると考えられている。本症例では、セレン欠乏の診療指針2024に基づく診断基準を満たしており、クローン病の腸管切除歴および透析導入によってセレン欠乏を呈し、拡張型心筋症を発症したと考えられた。
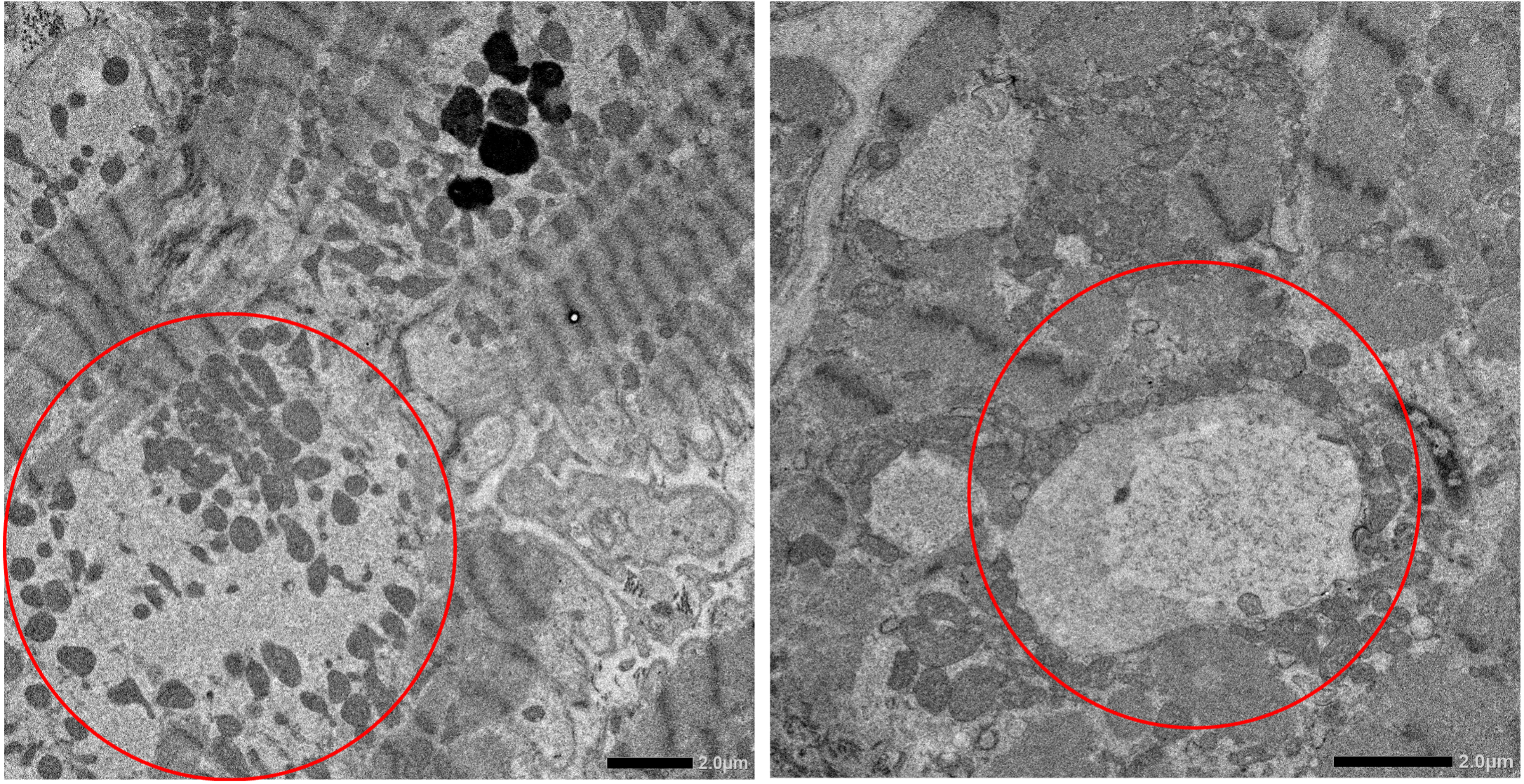
心機能障害のメカニズムとしては、セレン欠乏により抗酸化酵素であるグルタチオンペルオキシダーゼの働きが低下し、その結果、心筋細胞内で活性酸素が増加し、心筋細胞のアポトーシスやネクローシスを引き起こすとされている。心筋生検では、心筋細胞の配列異常やサルコメアの脱落、空砲形成などが認められた。この所見はセレン欠乏性心筋症に矛盾しないものであり、セレン欠乏による心機能低下を裏付けるものであった。
本症例では、このように心筋細胞の顕著な変性が認められたが、セレンの補充により心機能が劇的に改善した。
【結語】
心筋細胞の顕著な変性を認めたセレン欠乏性心筋症に、その補充療法が奏功した症例を経験した。
【参考文献】
- 1)
- 日本臨床栄養学会. セレン欠乏症の診療指針2024. 日本臨床栄養学会雑誌. 2024;46(4).
- 2)
- Munguti, et al. Selenium deficiency and its implications: A case report and review. Cureus. 2017 Aug 29;9(8):e1627. doi:10.7759/cureus.1627.
Figure 電子顕微鏡検査画像