第266回関東甲信越地方会 受賞演題一覧(2022年12月10日開催)
第266回関東甲信越地方会 最優秀賞受賞演題(2022年12月10日開催)
Student Award
心房細動時に心房筋が心外膜脂肪組織に与える影響の解明
石川 紗佳1)、鈴木 杏奈1)、岩嵜 利奈1)、井原 健介2)、古川 哲史2)、笹野 哲郎1)
1)東京医科歯科大学 循環制御内科学
2)東京医科歯科大学 難治疾患研究所 生体情報薬理学
【背景】
肥満は心房細動のリスク因子であり、心臓周囲に存在する心外膜脂肪の厚さと心房細動の発生率および重症度との関係が報告されている。心外膜脂肪と隣接する心筋との間には明確な境界がないため、心外膜脂肪が多くのアディポサイトカインを分泌して、心房の炎症や線維化を誘発して心房リモデリングを促進することが報告されている。一方、心房筋細胞が心外膜脂肪に及ぼす影響については未だ不明である。本研究では、心房細動を模した状態下で、心房筋細胞が脂肪細胞に及ぼす影響について、細胞外小胞の関与に着目して検討した。
【方法】
マウス線維芽細胞(3T3L1)より分化した脂肪細胞、マウス心房筋細胞(HL-1)はトランスウェルを用いて培養した。上に脂肪細胞下にHL-1細胞を培養し、二つの細胞が直接接しない状態で共培養した。HL-1細胞に10Hzの電気刺激を与え、共培養後に脂肪細胞中の炎症性サイトカインを定量RT-PCRで評価した。また、HL-1細胞から培地中に放出された細胞外小胞は沈澱凝集法を用いて抽出し、レーザー回折散乱法より大きさと個数を測定した。また抽出された細胞外小胞を脂肪細胞やマクロファージに添加して炎症性サイトカインを定量評価した。
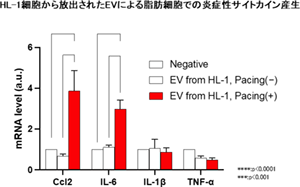
【結果】
HL-1細胞を脂肪細胞と共培養した状態でHL-1細胞に高頻度電気刺激を与えると、脂肪細胞における炎症性サイトカインの発現が上昇した。HL-1細胞から脂肪細胞に炎症のシグナルを伝える体液性因子の一つとして細胞外小胞の関与が考えられた。HL-1細胞に対して高頻度刺激すると、培地中への細胞外小胞の放出が刺激していない時と比べ増加した。HL-1細胞由来の細胞外小胞を抽出して脂肪細胞に添加しても共培養時と同様に炎症性サイトカインの発現増加が観察された。
【結語】
心房筋細胞は高頻度刺激により細胞外小胞を放出し、脂肪細胞の炎症の一部を誘導した。脂肪細胞と心筋細胞のクロストークが、心房細動をさらに進展させる可能性が考えられた。


Resident Award
心不全入院は全死亡・心血管死亡の代替となりうるか; RCTのメタアナリシス
清原 悠嵩1)、宮本 佳尚2)、岩上 将夫3)、Alexandros Briasoulis4)、工野 俊樹5)
1)横浜労災病院
2)国立がん研究センターがん対策研究所
3)筑波大学
4)University of Iowa
5)Montefiore Medical Center
【背景】
心不全入院は臨床試験の評価項目として用いられることがあるが、死亡の代替指標であるかは不明である。本研究では、心不全入院と死亡の相関についてメタアナリシスで検討した。
【方法】
PubMedにおいて、2022/4/13までに3大ジャーナル(NEJM, Lancet, and JAMA)に掲載されたランダム化比較試験(RCT)を対象として文献検索を行った。なお、心不全入院と死亡(全死亡もしくは心血管死亡)が主要・二次評価項目に含まれたRCTのみに限定した。RCT毎に治療介入による心不全入院、死亡に対する対数オッズ比をそれぞれX軸・Y軸にプロットし、その決定係数(R2)を算出した。R2 ≧ 0.7の場合には、強い代替指標であるとされる。また、観察期間(> 24ヶ月 vs. ≦24ヶ月)と患者背景(心不全患者 vs. その他)、介入方法(薬物介入 vs. その他)のそれぞれの条件を満たすRCTのみを対象にしてサブ解析を行った。
【結果】
120個のRCTが組み入れられた。心不全入院と全死亡のR2は0.41(95%信頼区間; 0.26, 0.56)、心不全入院と心血管死亡のR2は0.20(95%信頼区間; 0.05, 0.34)であり、心不全入院は死亡の弱い代替指標だった。サブ解析では、以下の3つの場合においては、心不全入院は死亡の中程度の代替指標であると判明した。1)観察期間が24か月よりも長期間のRCTに限定した場合(R2 = 0.58(95%信頼区間; 0.41, 0.75))、2)心不全患者を対象にしたRCTに限定した場合(R2 =0.55(95%信頼区間; 0.39, 0.72))、 3)薬物介入のRCTに限定した場合(R2 = 0.51(95%信頼区間; 0.35, 0.67))。また、観察期間が24ヶ月よりも長期であり、心不全患者に対して薬物治療で介入したRCTに限ると、心不全入院は死亡の強い代替指標だった(R2 = 0.80(95%信頼区間; 0.62, 0.97))。
【結論】
心不全入院は死亡の弱い代替指標だった。 心不全入院を死亡の代替指標とする妥当性は、臨床試験の観察期間と患者背景、介入方法に依存することが判明した。今後の臨床試験では、観察期間と患者背景と介入方法に基づいて、代替指標としての妥当性を判断することが可能である。

Clinical Research Award
ST上昇型急性心筋梗塞における責任病変プラーク性状と側副血行の発達の関係
山上 洋介1)、木村 茂樹1)、角田 貴大1)、宮﨑 紘子1)、三須 彬生1)、立石 遼1)、山口 正男1)、
加藤 信孝1)、島田 博史1)、一色 亜美1)、清水 雅人1)、藤井 洋之1)、鈴木 誠1)、笹野 哲郎2)
1)横浜南共済病院循環器内科
2)東京医科歯科大学循環器内科
目的;急性心筋梗塞における責任病変の性状と側副血行路の発達の関係を検討した。
方法;ST上昇型急性心筋梗塞の連続80症例で責任病変の性状をOCTで評価し、側副血行路との関連を検討した。本研究で特徴的な病変の性状として、同一プラーク内に層状構造とマクロファージを認めるものを、「マクロファージの集簇を伴うLayered plaque」と定義した。側副血行路の評価はRentrop分類で行い、Rentrop2または3を発達群、Rentrop0または1を未発達群として2群間の比較を行った。
結果:側副血行路の発達群は20%であった。また、発達群では未発達群に比較して、狭心症を先行する症例(68.8% vs. 29.7%, p=0.004)及びTIMI-0,1の症例(75.0% vs 31.2%, p=0.001)が多く、Minimum LumenDiameter(mm)は小さく(0.2±0.3 vs. 0.6±0.5, p=0.004)、%Diameter Stenosisは高値(91.0±12.9 vs. 79.4±16.5, p=0.005)であった。そして、発達群では、マクロファージの集簇を伴うLayered plaqueを有意に多く認めた(75.0% vs. 42.2%, p=0.019)。多変量解析ではマクロファージの集簇を伴うLayered plaqueは発達した側副血行路の独立した予測因子であった(OR: 6.48; 95%CI: 1.36-30.92; p=0.019)。
考察;側副血行路の形成には炎症の関与が不可欠であり、単球及び単球が分化したマクロファージは中核的役割を果たす。マクロファージの集積は、マクロファージ遊走阻止因子(Macrophage migration inhibitory factor: MIF)が強く発現している部位で認められる。MIFは短時間の心筋虚血でも放出され、虚血ストレス下のプレコンディショニングを促進する。Layered plaqueの形成過程で生じる短時間の虚血によりMIFが放出され、マクロファージの集簇が促進し、側副血行路の発達につながると考えられた。
結語;本研究は、側副血行路の発達と、責任病変のマクロファージの集簇の関係をOCTで示した初めての研究である。STEMIにおける責任病変の進行の機序と側副血行路の形成との関連を解明する上で重要な所見と考えられた。

Case Report Award
COVID-19 mRNAワクチン3回目接種後に劇症型心筋炎を発症した高齢女性の一例
関 侑華1)、樋口 亮介1)、七里 守1)、吉澤 佐恵子2)、磯部 光章1)
1)榊原記念病院 循環器内科
2)東京女子医科大学病院 病理診断科
【症例】
特記既往のない71歳女性が3回目のmRNA COVIDワクチン接種17日後に胸痛及び呼吸苦を主訴に受診。レントゲンでは肺鬱血あり、採血にてNT-proBNP上昇、血清トロポニンT陽性であった。SARS-CoV2ウィルスPCRは陰性、その他ウィルス抗体・抗原は陰性で、SARS-CoV2 spike抗体は陽性であった。心臓超音波検査にて基部下壁の菲薄化・瘤化と心尖部のakinesisが認められ、左室駆出率(LVEF)の低下(37%)、右室fractional area change(FAC)の低下(21.1%)を認めた。冠動脈に有意狭窄はなかった。心筋生検から急性リンパ球性心筋炎と診断した。ステロイドパルス療法にも関わらず心原性ショックに至り、IABPとECMOを導入した。その後血行動態は安定化し、第10病日にはPCPS、IABPから離脱し、第46病日に自宅退院した。2ヶ月後の心筋生検では膠原繊維が著明に増加し、間質への炎症細胞浸潤は減少していた。間質のIgGも初回と比較し減少していた。一方、CD68陽性macrophageの間質への浸潤は初回生検時よりも明らかに増加していた。4ヶ月後の経胸壁心エコーにおいて両室機能は大幅に改善していた(LVEF:53%、右室FAC:34%)。
【考察】
新型コロナウィルスmRNAワクチン関連心筋炎及びその激症化に至る機序について詳細は未だわかっていない。激症化したワクチン接種後心筋炎ではさまざまな病理像を呈することが知られている。巨細胞性心筋炎や好酸球性心筋炎の病理像を呈するものもあるが、本症例のようにリンパ球性心筋炎の病理像を呈するものが多い。3回目のコロナワクチン接種後の心筋炎の報告はこれまで1件のみで、本症例と同じく激症化した症例である。その症例においても急性期にはTリンパ球の浸潤が主体である点、マクロファージの浸潤が少数である点は同じである。加えて、本症例ではIgG発現が急性期に多く経時的に減少していること、CD1q発現が急性期において極めて少ないことが確認された。また、回復期に移行するにつれ、CD68陽性マクロファージ数の増加と間質繊維化の進行が同時に見られた。複数回の新型コロナウィルスmRNAワクチン接種による心筋炎の発症機序として、自然免疫応答よりも、記憶免疫細胞による獲得免疫機構の過剰活性化が心筋障害に関与しており、自然免疫系細胞の中でもマクロファージは炎症期よりも回復期において組織修復や組織繊維化に大きく関与している可能性が示唆される。



