第254回関東甲信越地方会 最優秀賞受賞演題(2019年12月7日開催)
Student Award
甲状腺機能亢進症の発症を契機に冠攣縮性狭心症を合併した1例
小柳 唯1)、小貫 龍也2)、正司 真2)、荒井 研2)、後閑 俊彦2)、豊崎 瑛士2)、関本 輝雄2)、松本 英成2)、
木庭 新治2)、新家 俊郎2)
1)昭和大学医学部5年
2)昭和大学医学部内科学講座 循環器内科学部門
【背景】甲状腺機能亢進症の心合併症として、心房細動や高心拍出性心不全の報告は多く見受けられる。しかし、冠攣縮性狭心症に関しては報告が少なく、その因果関係については異論も多い。
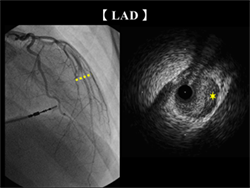
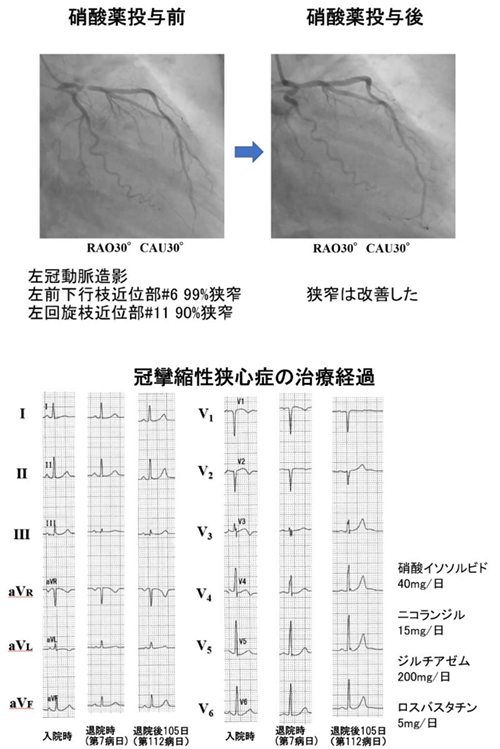
【症例】43歳女性。201X年Y月Z日に胸部絞扼感、動悸を認め当院受診した。血液検査で甲状腺機能亢進を認め、バセドウ病の診断でビソプロロール、チアマゾール、ヨウ化カリウムを投与した。5日後、突然の胸痛が出現し来院。血液検査で心筋逸脱酵素の上昇と、心電図で胸部誘導のST上昇を認め、緊急冠動脈造影検査を施行した。冠動脈造影は左前下行枝近位部に99%狭窄、左回旋枝近位部に90%狭窄を認めた。硝酸薬の複数回冠動脈内投与で、徐々に狭窄病変の改善を認め有意狭窄病変を残さなかったため、冠攣縮性狭心症と診断した。ビソプロロールを中止し、冠血管拡張薬、Ca拮抗薬を投与し、冠攣縮の再発なく経過し独歩退院となった。
【考察】今回の冠攣縮性狭心症の発症メカニズムとしては、2つ考えられる。1つ目は、本症例が重度の喫煙者(20歳より1日13本の喫煙歴あり)であったため、喫煙により血管内皮細胞の機能が障害され、NOの低下により血管平滑筋細胞の弛緩反応が低下していた点。2つ目は、甲状腺機能の亢進による甲状腺ホルモンの過剰のため、血管平滑筋細胞のα受容体の反応性がβ受容体に比して上昇することで、平滑筋細胞の収縮反応が亢進した点である。さらに甲状腺機能亢進症の治療薬としてβ遮断薬を投与していたため、収縮反応がより亢進しやすい状態だったと考えられる。また、甲状腺機能亢進症を合併する冠攣縮性狭心症の特徴として左冠動脈主幹部の攣縮、女性、50歳未満の症例が多いことが分かっている。さらに、甲状腺機能の正常化に伴い、冠攣縮はコントロール良好になることが報告されている。本症例でも、甲状腺ホルモンの値が低下するに伴い胸部症状が速やかに改善している。また、当院での冠攣縮性狭心症と甲状腺機能亢進症の合併例を調べたところ、2001から2017年に来院した冠攣縮性狭心症の症例520例のうち、甲状腺機能亢進症を発症していたのは2例であり、割合としては非常に少ないことが分かった。
【結論】甲状腺機能亢進症は、心房細動、心不全だけでなく、様々な心合併症を起こす事があり注意が必要である。甲状腺機能亢進症の患者にβ遮断薬を投与する際は、冠攣縮性狭心症のリスクファクターを評価したうえで慎重に投与する必要がある。
Resident Award
心室細動にて救急搬送されBarlow症候群の診断に至った一例
福岡 眞梨1)、北條 林太郎2)、前田 宗一郎2)、辻畑 志帆子2)、竹田 康佑2)、中村 真2)、山岡 広一郎2)、
新井 智之2)、川尻 紘平2)、田邉 翔2)、古谷野 康記2)、時岡 紗由理2)、稲垣 大2)、吉田 精孝2)、
河村 岩成2)、永嶺 翔2)、北村 健2)、土山 高明2)、深水 誠二2)、渋井 敬志2)
1)東京都立広尾病院 初期研修医
2)東京都立広尾病院 循環器科
症例は33歳女性。会食中に痙攣、意識障害を認めたため当院に救急搬送された。来院時心室細動(VF)を認めており経皮的心肺補助装置を装着し電気的除細動にて自己心拍再開に至った。冠動脈造影検査では有意狭窄を認めなかったが、左室造影検査ではSellers分類IV度の僧帽弁逆流を認めた。心臓超音波検査では僧帽弁が両尖に容積の増大と肥厚を伴い、腱索を牽引しながら左房へ逸脱するBillowing valveの所見であった。Holter心電図やモニター心電図では多源性の非持続性心室頻拍がみられ、加算平均心電図では心室遅延電位が陽性であった。各種薬剤負荷試験は異常なく、心臓MRI検査では左室遅延造影を認めなかった。以上の精査から、Barlow症候群によってVFを発症した可能性が示唆された。心臓電気生理学検査では左室に異常電位を認めなかったが、右室心尖部からの2連期外刺激でVFが誘発され、カテーテルの刺激でも容易にVFが誘発された。その後僧帽弁形成術及び人工弁輪を用いた弁輪縫縮術を行った。術後、突然死の二次予防目的に皮下植込み型除細動器を植え込み、β遮断薬を導入の上退院とした。
Barlow症候群は、高度な粘液腫様変性による両尖の肥厚、弁輪拡大を特徴とした僧帽弁逸脱症を呈し、心室性不整脈を認め、失神や胸痛、動悸など何らかの症状を示す症候群である。年齢は多くが60歳以下と若く、性差はないといわれ、一部に遺伝性が認められているが大部分は孤発性である。若年女性の突然死の原因として報告されているものの、その認知度が高いとはいえない。突然死の危険因子としては左室筋の線維化や多源性、右脚ブロック(RBBB)型など複雑型の心室性不整脈、女性、両尖の逸脱、Mitral Annular Disjunctionなどが指摘されており、本症例でも複数の危険因子(下図 ②、③、④、⑥、⑦に該当)を認めた。
Barlow症候群に関する精査や治療は確立されていないが、突然死を念頭に置いた積極的なリスクアセスメントを進めていくべきだと考える。

Clinical Research Award
心電同期CTを用いた肺高血圧症における新しい右室形態評価の試み重症度、予後そして右室心筋性状への影響
土橋 正弥1)、船橋 伸禎2)、小澤 公哉2)、小林 欣夫2)、田邉 信宏3)、巽 浩一郎3)
1)千葉大学医学部医学科3年
2)千葉大学循環器内科学
3)千葉大学呼吸器内科学
背景:右室肥大では12誘導心電図のV1誘導でR/S>1などが知られている。右室肥大をきたす代表疾患には肺高血圧症(PH)などが挙げられる。経胸壁心エコーでは著明に拡大、肥大した右室を明瞭に描出するのは困難なことがあるが、心臓CTは容易に右室全体像を描出できる。さらに心電同期CT上ではPH症例において右室流出路優位型肥大と右室び漫性型肥大が観察されるとされているが(図)、両者の臨床的意義はまだ不明である。
目的:PH症例における右室肥大の解剖学的2つの形態:“右室流出路優位型”と“右室び漫性型”を心臓CTで診断し、両者の心電図所見、重症度、右室心筋性状そして予後への影響を評価する
対象と方法:対象:心電同期CT、心電図、心エコー、血漿脳性ナトリウム利尿ペプチド(BNP)測定を3か月以内に施行した総計43名のさまざまな背景、原因のPH症例(女性33例、年齢5515歳)右室肥大はCTで拡張末期壁厚5mm以上と定義した。症例をCT上①右室流出路優位型肥大(6例)、②右室び漫性型肥大(26例)、③右室肥大無し(11例)と3群に分類した。PH重症度は血漿BNP、心エコーで計測される肺動脈収縮期圧(三尖弁逆流より推定)、右室心筋性状評価として、心臓CTでの右室心筋線維化、そして予後として原疾患由来の死亡発生をイベントとした。
結果:3群間に年齢、性別の割合、背景疾患の割合に有意差はなかった。観察期間中、右室流出路優位型、び漫性型、肥大無の3群で0、2、1例が死亡し、3群間にKaplan Meier解析とlog rankテストで有意差は無かった。右室肥大がある32例中(右室流出路優位型PH6例とび漫性型PH26例)の2群間の比較で右軸偏位、右脚ブロックの頻度、QRS幅、右脚ブロック症例を除いた症例でのV1でのR/S比、最大右室壁厚(CT)、血漿BNP、推定肺動脈収縮期圧(心エコー)に有意差は無かった。右室流出路優位型のみで最大右室壁厚(CT)と血漿BNP、最大右室壁厚(CT)と推定肺動脈収縮期圧に弱い正の相関がみられた。(び漫性型は無相関)。右室流出路優位型はび漫性型より右室心筋線維化の頻度が有意に高率であった。
結語:さまざまなPH症で右室流出路優位型肥大、び漫性型肥大は類似した重症度と予後を持つが、右室心筋線維化が前者で高率であり、また両型間に、最大右室壁厚と血漿BNP、最大右室壁厚と推定肺動脈収縮期圧の相関に相違がみられた。両者は解剖学的、心筋性状に明らかな違いを示し、PH症のリスク層別化などに有用となる可能性を考え、今後も検討していきたい。

Case Report Award
デスミン遺伝子異常を伴う左室緻密化障害に繰り返す特発性冠動脈解離を合併した一例
田宮 蘭、齋藤 佑記、深町 大介、永嶋 孝一、相澤 芳裕、村田 伸弘、阿久津 尚孝、奥村 恭男
日本大学医学部内科学系循環器内科学
デスミンは骨格筋、心筋、平滑筋で発現する中間径フィラメントタンパク質の一種である。デスミン関連ミオパチー(DRM)はデスミン遺伝子変異により生じ、多くは常染色体優性遺伝である。骨格筋の衰弱、伝導障害、拡張型心筋症などを特徴とするが、その表現型は完全には明らかにされていない。
症例は22歳女性。小児期より低心機能と進行性伝導障害を指摘されていた。20歳時に胸痛のため救急搬送された際に、心臓超音波検査で左室緻密化障害であると診断された。緊急冠動脈造影検査では、左前下行枝(LAD)#6に高度狭窄を認めた。血管内超音波で特発性冠動脈解離(SCAD)と診断され、経皮的冠動脈形成術が施行された。1年後、再度胸痛が出現した。冠動脈CT検査にてLAD末梢に狭窄が認められた。SCADの再発と考えられ、保存的に加療を行った。数か月後心不全が増悪し、強心薬、機械的補助循環依存状態となったため、左室補助人工心臓植込みを施行した。現在は退院され、移植待機中である。本症例は小児期に遺伝子検査を行ったが、長い間変異が同定できなかった。しかし、DNAシークエンス技術の発達により、デスミン遺伝子でミスセンス変異が判明した。両親と弟の遺伝子検査の結果から、本症例がde novo突然変異であると考えられた。
本症例から3つの知見が得られた。第1に本症例はDRMにSCADを合併した初の報告である。マウスでは、デスミン遺伝子変異により血管中膜の破壊や血管平滑筋の形成不全が引き起こされたという報告がある。SCADの剖検例では血管平滑筋の消失や、中膜の解離を示したという報告がある。DRMの患者が突然の胸痛を訴えた場合、血管平滑筋に異常をきたすSCADを考慮する必要があると思われる。第2にDRMの心筋の表現型として拡張型心筋症、肥大型心筋症、拘束型心筋症が明らかとなっているが、本症例からDRMの新たな表現型として左室緻密化障害が含まれる可能性が示唆される。第3にDRMは骨格筋の衰弱や家族歴がない場合にも考慮する必要があると考えられる。
本症例は、de novoデスミン遺伝子変異を伴う筋症状がない若年女性に、左室緻密化障害と2回のSCADを合併し、心不全のコントロールに難渋した極めて稀有な一例と考えられる。