第251回関東甲信越地方会 最優秀賞受賞演題(2019年2月2日開催)
Student Award
女性ホルモン補充療法の冠動脈イベント発症に対する年齢別影響;メタアナリシス
松本卓也1)、小寺聡2)、篠原宏樹2)、清末有宏2)、安東治郎2)、赤澤宏2)、小室一成2)
1)東京大学医学部医学科5年
2)東京大学医学部附属病院 循環器内科
【Backgrounds】循環器内科学の教科書執筆にあたり、性差が動脈硬化に及ぼす影響を調べていた。女性ホルモン補充療法(HRT)によって心血管イベントが増加すると報告されていたが、年齢やホルモンの種類によって、その影響は変わることが示唆されている。HRTの冠動脈性心疾患(CHD)に対する有用性を年齢別・ホルモンの種類別に検討しようと思い、メタアナリシスを試みた。
【Methods】
Information Source:Pubmed, Cochrane
Search:”Hormone Replacement Therapy”, “Coronary Disease”, ”Postmenopausal"
Inclusion Criteria:女性に対するHRTのRCT、EndpointにCHDを含む
Exclusion Criteria:担癌患者を対象としたStudy
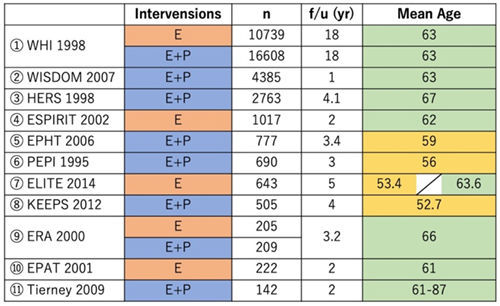
集めたstudyを、Estrogen単剤かEstrogen+Progesterone合剤か、60歳未満か以上かの4群に分け、それぞれForest Plotで検討を行った。Primary EndpointにはCHD、Secondary EndpointにはCardiovascular Death、Total Deathを設定した。
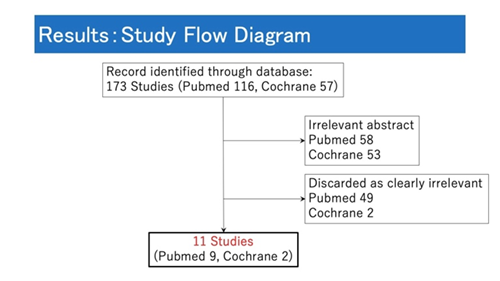
【Results】173のstudyから11のstudyが選別され、38800人の患者データが集められた。Estrogen単剤のプラセボに対するCHD発症のOdds Ratioは、60歳未満で0.58 [95% Confidence Interval 0.32-1.05]、60歳以上で0.93 [95%CI 0.79-1.09]であった。Estrogen+Progesterone合剤のプラセボに対するCHD発症のOdds Ratioは、60歳未満で1.18 [95%CI 0.75-1.85]、60歳以上で0.99 [95%CI 0.83-1.18]であった。Secondary Endpointでは、60歳未満に対するEstrogen単剤投与がTotal Deathの抑制効果を示した(OR 0.77 [95%CI 0.62-0.95])が、それ以外の群では、結果はneutralであった。
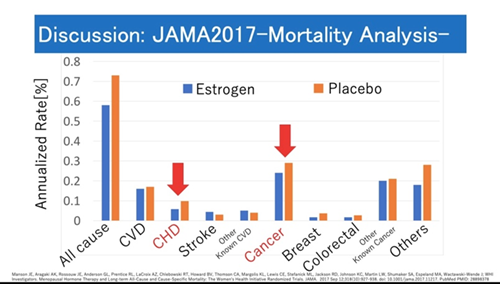
【Discussion】60歳未満のEstrogen単剤投与群がなぜ他と異なる結果となったのか考察するため、最も影響の大きかったJAMA2017のStudyに注目した(Weight 96.6%)。同群の死亡原因を解析した結果、CHDやCancerが抑制傾向を示しており、これらが累積した結果、Total Deathが有意に抑制されたと考えられる。なお、このstudyでは、子宮摘除後の患者にEstrogen単剤、子宮がある患者にEstrogen+Progesteroneの合剤を投与する標準治療を施行していた。
このEstrogenの効果の年齢差は、動脈硬化の進展度合いにより、発現するEstrogen Receptorの種類が変わるからだと考えられている。閉経直後の若い人の血管では、ERαが優位に発現しており、この場合、Estrogenは動脈硬化を抑制するように働く。一方、閉経から時間が経った人の血管では、ERβが優位に発現しており、この場合、Estrogenは動脈硬化を促進するように働く。
【Conclusion】CHDに対する有用性が確認できたHRTは、60歳未満の患者に対するEstrogen単剤投与のみであった。ただし、子宮摘出後を対象としていたことには留意しなければならない。
Resident Award
ウイルス性心筋炎に難治性の冠攣縮性狭心症を合併した稀な一例
濱野頌子、岡崎徹、三宅渉、工藤綾子、葉山裕真、中村友妃子、久保田修司、粟屋徹、中川堯、
山本正也、岡崎修、原久男、廣井透雄(国立国際医療研究センター 循環器内科)
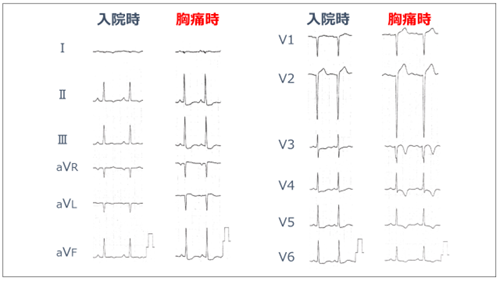
症例は、21歳中国人男性である。発熱、呼吸困難を主訴に入院となった。血液検査で炎症反応が高値であり、トロポニンおよびBNPの上昇を伴った。心電図上V1-V2のST上昇があり、心エコーで心尖部を中心とした左室の壁運動障害を認めた。冠動脈造影では3枝末梢領域の狭小化があったが、治療を要する狭窄所見は認められなかった。左室造影ではたこつぼ心筋症様の心尖部収縮不良が著明であった。心筋MRI画像では、T2 STIRで前側壁全層の浮腫性変化を認めた。LGEでは中間部の前壁~心尖部にかけて心内膜下に遅延造影を認めた。アデノウイルス5型抗体が陽性で、心筋生検結果心筋周囲のリンパ球浸潤像があり、リンパ球性心筋炎の診断となった。
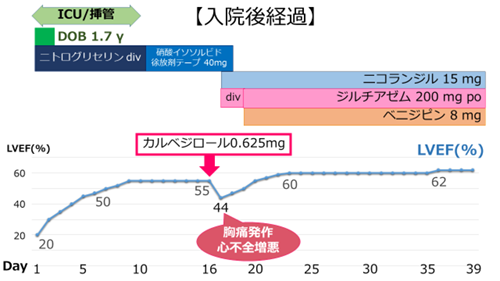
CS1 の急性心不全として挿管、ICU入室となりニトログリセリンと利尿剤で加療後volume reductionが得られ抜管となった。心尖部収縮不良は遷延し、第15病日より頻脈を認め、頻脈を伴う低左心機能に対しβblockerを投与開始した。同日夜間から早朝にかけて胸痛症状が出現し、心不全の再増悪をきたした。発作時心電図で前胸部誘導のST変化を認め、トロポニンの上昇を伴い、臨床的に冠攣縮性狭心症発作と診断した。βblockerを中止のうえ、カルシウム拮抗薬の投与を開始した。最終的に症状安定までに血管拡張剤に加えカルシウム拮抗薬2剤を要し、第39病日で退院となった。
心筋炎に冠攣縮性狭心症を併発した症例が少数報告されている。心筋炎に冠攣縮が併発する機序として、感染に伴う血管内皮細胞障害によるNO合成低下と、Rhoキナーゼ亢進を介した血管平滑筋化収縮の二つの機序が考えられ、心筋炎が冠攣縮を誘発するリスクとなることが示唆される
Clinical Research Award
肥大型心筋症と妊娠・出産
桂木真司1)、高山守正2)、高見澤格2)、磯部光章2)、高梨秀一郎3)
1)榊原記念病院 産婦人科
2)榊原記念病院 循環器内科
3)榊原記念病院 心臓血管外科
これまで閉塞性肥大型心筋症(HOCM)は左室流出路閉塞例では妊娠後期、分娩後に合併症発現が多く出産を回避されてきた。しかし多科協力による早期の適切な診断と、薬物ならびに中隔縮小治療により良好な状態への回復が可能であり、挙児希望を実現できる。受診された肥大型心筋症の患者は、肥大型心筋症カンファレンスで相談され、出産希望の女性16名が循環器内科・心臓外科で治療した後に産科へ紹介、うち12名が妊娠された。
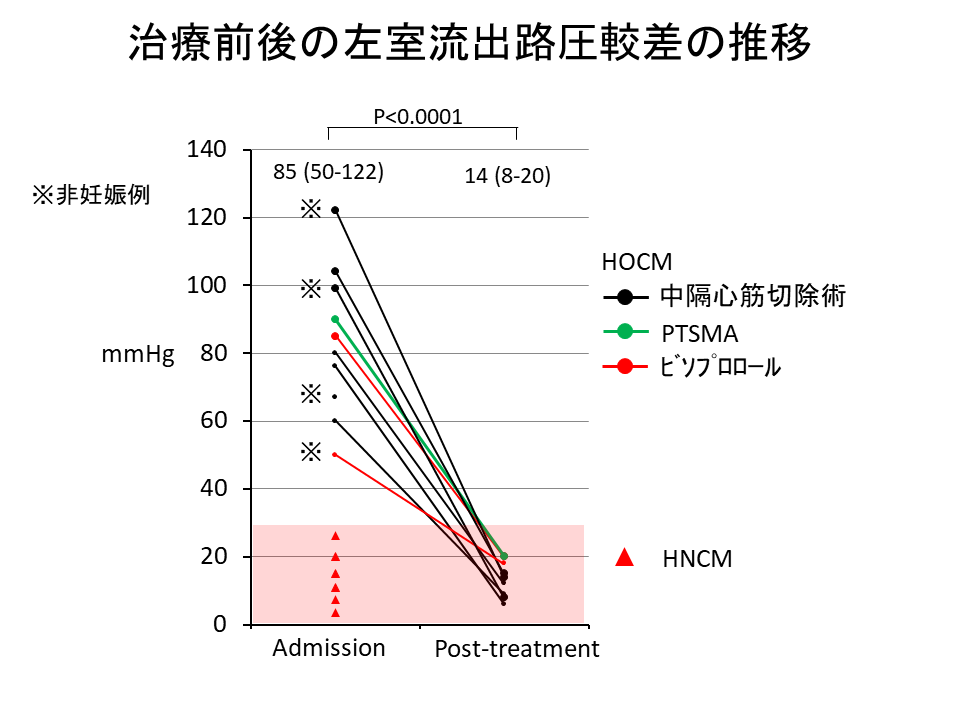
妊娠前に薬剤治療(12名)、中隔心筋切除術(7名)、中隔心筋焼灼術(1名)を行い、左室流出路圧較差は平均85mmHgから14mmHgに下がり、NYHAクラス分類もクラスⅡmからクラスⅠに改善した。うち1名は流産され、1名は早産、10名が満期産で2500~3200gの元気な新生児が生まれた。11名中8名はビソプロロール内服を続け心不全を防止したが、薬剤の母児への副作用なく、さらに妊娠中の心合併症は妊娠37週で心拡大・一過性心房細動が1名、出産後に非持続性心室頻拍・心拡大が1名あり、いずれも利尿剤のみで軽快した。
危険とされる、圧較差>30mmHg以上の閉塞型肥大型心筋症も関連チームによる十分な検討と事前の治療、つまりβ遮断薬中心の薬物治療、さらに薬に不応な心不全症状へは中隔心筋切除術などの専門的外科的治療が奏功し、大多数が安全に満期出産を行えた。

Case Report Award
心原性ショックの症例に対し、V-A ECMOとImpellaを併用した際の流量設定と心エコーでの評価について
佐藤啓、矢作和之、瀬戸口尚登、渡辺悠介、中瀬将明、中村公亮、田村佳美、菊島朋生、冨井大二郎、
中西亨、二宮開、小関啓太、田中徹、小池秀樹、阿佐美匡彦、田中旬、小宮山浩大、青木二郎、田邉健吾
(社会福祉法人 三井記念病院 循環器内科)
【症例】非ST上昇型急性心筋梗塞の診断で冠動脈バイパス術を施行された70歳男性。術後心原性ショックを合併していたためV-A ECMOとImpella 5.0を併用(EC-PELLA)した。ECMOとImpellaを併用した場合の最適な流量設定方法は明らかになっていない。本症例ではECMOとImpellaの流量を変更した際の、血行動態の変化と心エコーでの左室機能指標の変化について考察した。ECMOの流量を上げると平均血圧は上昇し、左室収縮末期容積が増大した。一方で、Impellaの流量を上げると平均血圧は軽度上昇に留まり、左室拡張末期容積が減少した。左室拡張末期容積の減少は左室の心筋酸素消費量の軽減が示唆され、左室機能の回復につながると考えられる(図1)。以上より、ECMOは循環サポートに長けるデバイスだが左心負荷を増大させる。一方で、Impellaは循環サポートにおいてはECMOと比較し劣るが、左心負荷軽減に長けたデバイスといえる。循環動態を維持できる最小限のECMO flowに、可能な範囲で最大限のImpella flowを組み合わせた設定が、より理想的なEC-PELLA設定といえる可能性が示唆された。ただし、肺血管抵抗増大や右心機能低下を合併した症例では、右心系から左心系への血液流入が低下するため、最大限のImpella flowでは左室の虚脱から不整脈を誘発し、却って血行動態を悪化させることがありえるため注意が必要である。
【結語】心原性ショックに対してECMOとIMPELLAを併用した症例を経験した。EC-PELLA管理の場合、肺血管抵抗を含む右心機能を考慮して、それぞれの流量設定を検討する必要がある。最適な流量設定は個々の症例によるが、指標として心エコー(EDV、ESV)やSwan-Ganzのデータが有用であった。
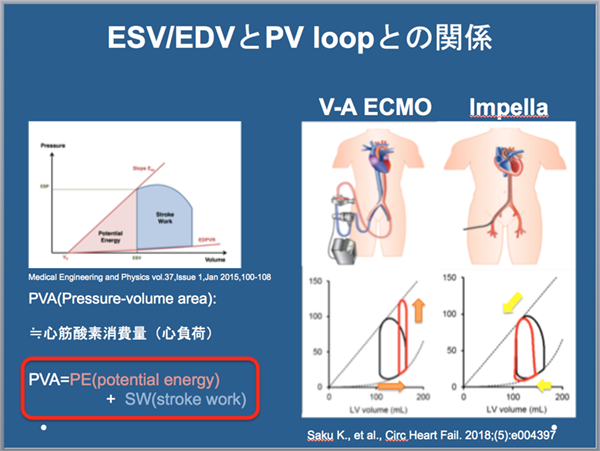
図1. PV loopにおいて、ECMOの流量を上げると左室収縮末期容積は増大し、血圧は上昇するが、PV loopは右上方へ偏位し心負荷は増加する。一方で、Impellaの流量を上げると血圧は著変ないが、左室拡張末期容積は減少し、PV loopは左下方へ偏位し心負荷は軽減する。

